Озон в природе и его производство
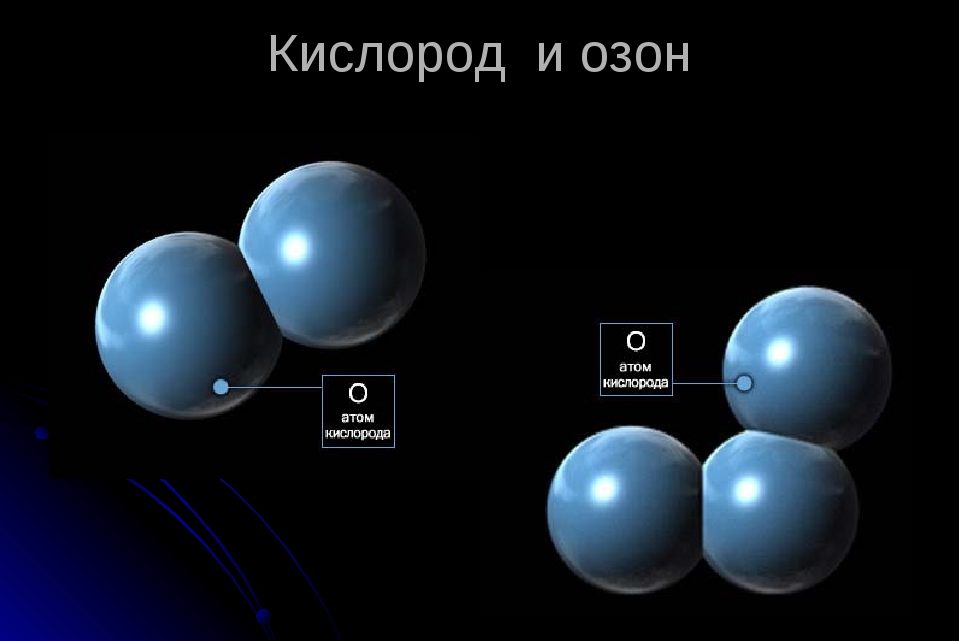
Озон (O3) — голубоватый газ с характерным резким запахом, который является сильным окислителем, вызывающим воспламенение паров спирта. Он был назван в честь судороги. слово озеин , означающее; тот, кто нюхает. Кислород встречается в природе, за исключением двухатомной молекулы, а также трехатомной молекулы O 3 . Кислород (O 2 ) и озон (O 3 ) являются аллотропными модификациями кислорода. Альтропическая модификация — это явление, при котором один и тот же элемент встречается в нескольких формах из-за способа связывания. Кислород имеет ковалентную двойную неполярную связь, а озон — тройную ковалентную связь.

Озон — это аллотропная модификация кислорода, молекулы которого состоят из трех атомов кислорода. Обе связи между атомами кислорода имеют одинаковую длину, что позволяет предположить, что в молекуле озона нет двойной связи, но что одна электронная пара окружает ядра всех трех ядер одновременно. Следовательно, в молекуле озона есть делокализованные электроны.
Резонансные структуры обозначают только один тип молекул с делокализованными электронами, а не смесь структурно разных молекул, которые быстро переходят друг в друга.
Когда летом после грозы наступает ясный и солнечный день, чувствуется запах «свежего воздуха». Пахнет озоном в очень малых концентрациях. Запах озона ощущается в воздухе уже при объемной доле 1 ppm.
Где находится озон
Озон в природе образуется в нижних слоях атмосферы (тропосфере) и в верхних слоях атмосферы (стратосфера; где его больше всего — на высоте 20-25 км от земли). В стратосфере он образуется из элементарного кислорода. Он поглощает ультрафиолетовое излучение Солнца , действие которого вредно для живых организмов. Без стратосферного озона жизнь на Земле была бы невозможна. Количество озона в тропосфере на первых 5 км над землей постоянно растет из-за увеличения трафика и промышленности.
Различные технологические достижения (например, реактивные самолеты), а также использование новых органических веществ привели к снижению концентрации озона. Следствием этого является истощение озонового слоя, то есть, как его образно называют, создание «озоновых дыр». Первые дыры были обнаружены над Антарктидой в 1985 году .
Озон обычно получают реакцией атомарного и молекулярного кислорода. Для получения атомарного кислорода необходимо подавать энергию, обычно в виде УФ-излучения или высокого переменного напряжения. В лаборатории его получают в озонаторах путем электрического разряда в атмосфере кислорода.
Смесь в трубке озонатора охлаждается, поскольку образующийся озон быстро разлагается. Объемная доля озона в смеси, полученной в озонаторе, составляет 15%. Чистый озон можно получить путем сжижения полученной смеси жидким воздухом и фракционной перегонкой.
За исключением озонатора (который чаще всего используется для очистки рек), озон можно получить в лаборатории путем реакции перманганата калия и концентрированной серной кислоты .
16 сентября отмечают Международный день озона .
Использование озона
Озон вреден для здоровья, потому что он раздражает органы дыхания, более высокие концентрации вызывают кровотечение из носа и головные боли, а также могут вызвать смерть. После фтора это самый сильный окислитель, поэтому его использование основано на этом свойстве. Он используется для стерилизации воды, операционных, кинотеатров и спортивных залов (для уничтожения микроорганизмов), затем в фармацевтической, косметической, полиграфической промышленности, а также в бумажной, текстильной и пластмассовой промышленности.
1987 г. Был принят Монреальский протокол — соглашение, по которому подписавшие страны обязуются сократить использование фреона на 50%.



